 Helicobacter pylori - o bacterie Gram (-), microaerofilă, de dimensiuni infime-constituie un adversar redutabil al celulelor epiteliale din mucoasa gastrică, “succesul” său fiind confirmat de “gazda” reprezentată de jumătate din populaţia lumii şi de etiologia unei game variate de afecţiuni gastrointestinale. Infecţia netratată determină modificări atrofice şi creează condiţii favorabile pentru evoluţia carcinomului, fiind prima bacterie identificată cu potenţial neoplazic. Procesul de colonizare este rezultatul colaborării dintre secreţia acidă a gazdei şi factorii de virulenţă ai bacteriei.
Helicobacter pylori - o bacterie Gram (-), microaerofilă, de dimensiuni infime-constituie un adversar redutabil al celulelor epiteliale din mucoasa gastrică, “succesul” său fiind confirmat de “gazda” reprezentată de jumătate din populaţia lumii şi de etiologia unei game variate de afecţiuni gastrointestinale. Infecţia netratată determină modificări atrofice şi creează condiţii favorabile pentru evoluţia carcinomului, fiind prima bacterie identificată cu potenţial neoplazic. Procesul de colonizare este rezultatul colaborării dintre secreţia acidă a gazdei şi factorii de virulenţă ai bacteriei.
 Este produsă ca o protoxină cu greutatea moleculară de 140 k-Da, urmând ca în momentul secreţiei să fie clivată în forma sa matură de 95 k-Da. Gena care o codifică este prezentă în toate subtipurile bacteriei, cea care variază fiind capacitatea de vacuolizare. Datorită heterogenitatăţii regiunilor s (codifică peptida semnal) şi m (conţine domeniul de legare al p58), aceasta este maximă pentru genotipurile s1/m1 (asociate cu ulcerul peptic si carcinomul gastric), medie pentru genotipurile s1/m2 şi absentă în cele s2/m2. Polimorfismul expresiei genei reflectă adaptarea continuă a bacteriei ce asigură persistenţa infecţiei.
Este produsă ca o protoxină cu greutatea moleculară de 140 k-Da, urmând ca în momentul secreţiei să fie clivată în forma sa matură de 95 k-Da. Gena care o codifică este prezentă în toate subtipurile bacteriei, cea care variază fiind capacitatea de vacuolizare. Datorită heterogenitatăţii regiunilor s (codifică peptida semnal) şi m (conţine domeniul de legare al p58), aceasta este maximă pentru genotipurile s1/m1 (asociate cu ulcerul peptic si carcinomul gastric), medie pentru genotipurile s1/m2 şi absentă în cele s2/m2. Polimorfismul expresiei genei reflectă adaptarea continuă a bacteriei ce asigură persistenţa infecţiei.
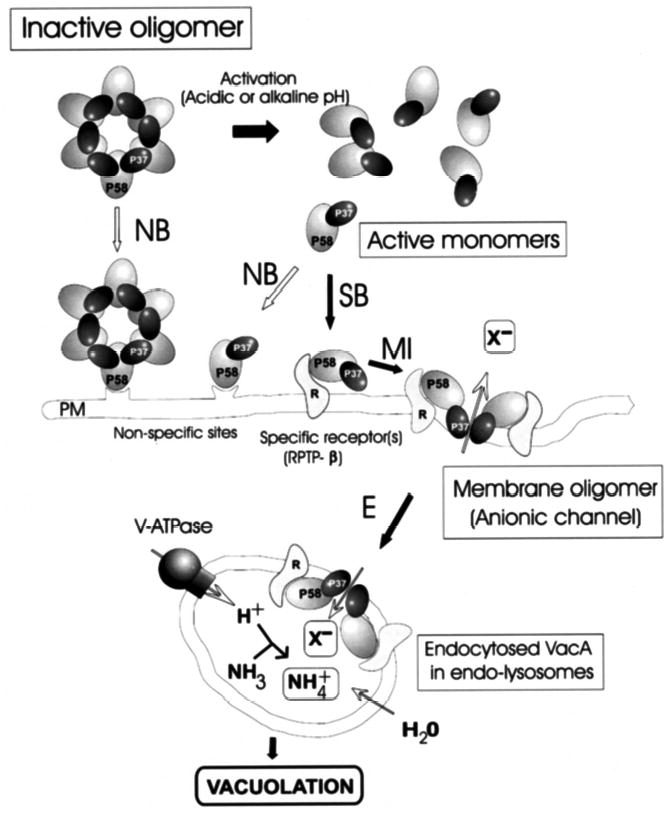
După secreţie, vacA este activată de mediul acid şi se leagă de receptorul tirozin fosfatazei β (RPTPβ) din membrana celulei gastrice. O parte din citotoxina secretată nu este eliberată în mediu şi rămâne ancorată de membrana externă a H. pylori, exercitându-şi activitatea toxică în urma viitoarelor contacte dintre bacterie şi celulele gazdei. Ulterior, prin clivare proteolitică se formează fragmentul N-terminal (33 kDA) care intervine în formarea canalelor anionice şi fragmentul C-terminal (55 kD) care mediază adeziunea celulară. Cele două fragmente rămân legate noncovalent şi pătrund în membrană, formând un por.
Apoi, moleculele de vacA sunt internalizate prin endocitoză mediată de receptori, transportate şi acumulate în endolizozomi. Sub acţiunea V-ATP-azei, aceştia devin un rezervor de baze slabe, determinând influxul apei şi apariţia fenomenului de swelling cu formarea vacuolelor (vezi fig.1). Astfel, procese importante pentru menţinerea homeostaziei celulare, precum transportul hidrolazei acide către lizozomi şi capacitatea de digestie intracelulară a acestora din urmă sunt sistate, fiind facilitată şi neutralizarea mediului acid de la nivel gastric.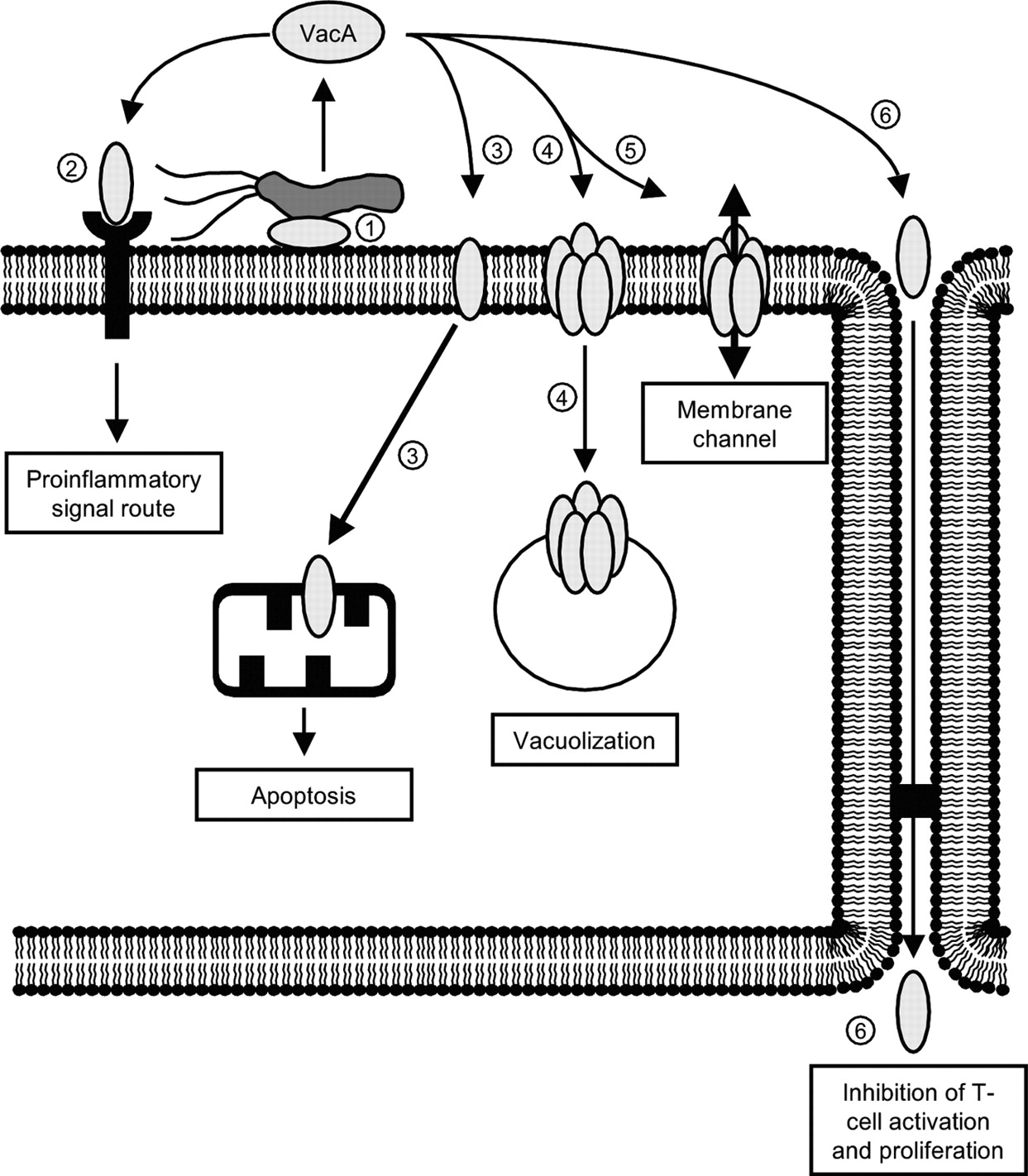 Tot la nivelul celulei gastrice, citotoxina poate forma pori în membrană, inducând eliberarea de uree şi de anioni. Prin crearea de canale anionice-selective (HCO3− ) în membrana apicală, reuşeşte încă o dată să neutralizeze aciditatea gastrică. De asemenea, alterează joncţiunile strânse, afectând integritatea mucoasei şi inducând efluxul de nutrienţi din mucoasă în stratul mucos. Prin urmare, creşte permeabilitatea transcelulară, determinând difuzia unor nutrienţi vitali precum Ni2+ şi Fe3+.
Tot la nivelul celulei gastrice, citotoxina poate forma pori în membrană, inducând eliberarea de uree şi de anioni. Prin crearea de canale anionice-selective (HCO3− ) în membrana apicală, reuşeşte încă o dată să neutralizeze aciditatea gastrică. De asemenea, alterează joncţiunile strânse, afectând integritatea mucoasei şi inducând efluxul de nutrienţi din mucoasă în stratul mucos. Prin urmare, creşte permeabilitatea transcelulară, determinând difuzia unor nutrienţi vitali precum Ni2+ şi Fe3+.
În sprijinul complexităţii patogenităţii, vine şi capacitatea imunomodulatoare susţinută de abilitatea citotoxinei secretate de a interacţiona cu celule imuno-competente ca : monocite, granulocite, limfocite B şi limfocite T. Contactul cu acestea la nivelul laminei propria este favorizat de alterarea joncţiunilor strânse, menţionată anterior. Totodată, prezintă chemotactism pentru mastocite, acestea producând citokine proinflamatorii (TNF- , IL-1 , IL-6, IL-10, IL-13), fără să aibă loc degranularea.
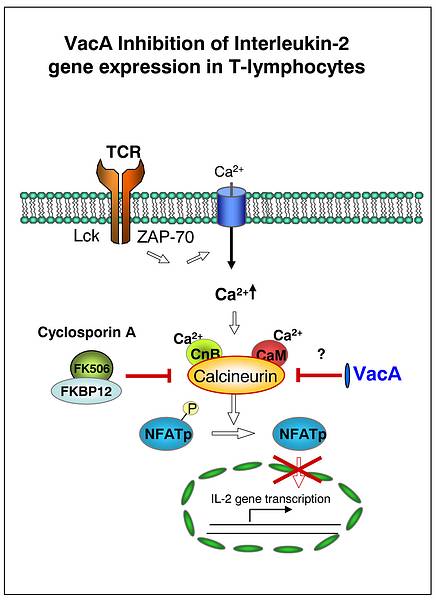 Dacă în urma interacţiunii cu limfocitele B reuşeşte să inhibe prezentarea antigenelor, asupra limfocitelor T determină inhibarea proliferării lor şi secreţiei de IL-2. Legându-se de subunitatea beta-2 integrina a receptorului CD18, opreşte activitatea fosfatazei calcineurina, dependentă de complexul Ca2+-calmodulină (vezi fig 3). Calcineurina activată, prin defosforilarea situs-urilor serin-treoninice ar fi realizat translocarea în nucleu a NFAT (familie de factori transcripţionali implicaţi în inducerea sintezei citokinelor). Mecanismul, asemănător celui de imunosupresie al ciclosporinei A, explică modul prin care Helicobacter pylori reuşeşte să evite răspunsul imun al gazdei.
Dacă în urma interacţiunii cu limfocitele B reuşeşte să inhibe prezentarea antigenelor, asupra limfocitelor T determină inhibarea proliferării lor şi secreţiei de IL-2. Legându-se de subunitatea beta-2 integrina a receptorului CD18, opreşte activitatea fosfatazei calcineurina, dependentă de complexul Ca2+-calmodulină (vezi fig 3). Calcineurina activată, prin defosforilarea situs-urilor serin-treoninice ar fi realizat translocarea în nucleu a NFAT (familie de factori transcripţionali implicaţi în inducerea sintezei citokinelor). Mecanismul, asemănător celui de imunosupresie al ciclosporinei A, explică modul prin care Helicobacter pylori reuşeşte să evite răspunsul imun al gazdei.În concluzie, citotoxina vacuolară sporeşte patogenitatea lui Helicobacter pylori, facilitând colonizarea acestei bacterii. Nu numai că are efecte directe asupra celulelor gastrice, fiind implicată în etiologia ulcerului peptic şi a gastritei cronice, dar prezintă şi proprietăţi imunomodulatorii, relevând capacitatea remarcabilă de cronicizare a lui Helicobacter pylori. Toate aceste caracteristici o transformă în candidatul ideal pentru un posibil vaccin, fiind o resursă inepuizabilă pentru cercetare.
Bibliografiehttp://www.ncbi.nlm.nih.gov/bookshelf/br.fcgi?book=hp∂=A974http://cmr.asm.org/cgi/content/full/19/3/449#VacA_vacuolating_cytotoxin.http://www.jbc.org/content/281/16/11250.abstracthttp://www.mvp.uni-muenchen.de/bacteriology-wg6-research.htmlhttp://www.jimmunol.org/cgi/content/full/168/6/2603sciencesignaling.org/cgi/reprint/sci;301/5636/1099.pdf
| < Anterior | Urmator > |
|---|








